Spletna revija za znanstvenike, strokovnjake
in nevroznanstvene navdušence
Naslovnica Članki Intervjuji Mnenja Zdravje Korenine eSinapsa Številke ![]()
Dostava terapevtikov preko krvno-možganske pregrade
članki
eSinapsa, 2011-1
Zvezdan Pirtošek
Eksoskeleti – inteligentne bionske naprave
Marko Munih
O aktualnih dilemah draženja globokih možganskih struktur pri obsesivno - kompulzivni motnji
Nadja Jarc
Sledite svojo srečo ... z iPhone
Urban Kordeš
eSinapsa, 2011-2
Renata Salecl
Gašper Tkačik
Astrociti – spregledane zvezde nevrobiologije
Marko Kreft, Robert Zorec
Sašo Dolenc
Meditacija - malo truda, veliko koristi
Luka Dimic
eSinapsa, 2011-3
Mara Bresjanac
Martina Starc
Rok Berlot
Varnost uporabe generičnih protiepileptičnih zdravil
Mojca Kržan, Matevž Kržan
Možgani, računalniki - nekaj vmes
Miha Pelko
eSinapsa, 2012-4
Ali so moški in ženski možgani različni?
Gregor Majdič
O kognitivnih motnjah pri bolnikih s Parkinsonovo boleznijo
Dejan Georgiev
Akutno možgansko kap lahko uspešno zdravimo
Nina Vujasinovič, Bojana Žvan
Vloga nevropsihološke diagnostike pri odkrivanju zgodnjih znakov alzheimerjeve bolezni
Simon Brezovar
eSinapsa, 2013-5
Novo odkritje na področju sporadičnih prionskih bolezni
Jana Jerše, Nadja Jarc
Učinek placeba brez lažnih zdravil in zavajanja
Mara Bresjanac
Subarahnoidna krvavitev zaradi tromboze venskih sinusov
Mateja Repar, Anita Resman Gašperčič
Srečanje dveh velikanov: možganov in imunskega sistema
Matej Markota
eSinapsa, 2013-6
Odstranjevanje možganskih tumorjev pri budnem bolniku
Andrej Vranič, Jasmina Markovič, Blaž Koritnik
Zmedena bolnica, ki nič ne vidi ali PRES
Manja Hribar, Vid Zgonc
Manja Hribar
Netravmatska lokalizirana konveksitetna subarahnoidna krvavitev
Mateja Repar, Fajko F. Bajrović
Sistemska skleroza in ishemična možganska kap - vzročna povezanost ali le koincidenca?
Mateja Repar, Janja Pretnar Oblak
Klemen Grabljevec
Z omejevanjem spodbujajoča terapija pri bolnikih po nezgodni možganski poškodbi
Dejana Zajc, Klemen Grabljevec
eSinapsa, 2014-7
Možgani v mreži navezanosti, ki nas zaznamuje
Barbara Horvat
Vpliv senzoričnega dotoka na uglasitev možganskih povezav
Peter Gradišnik
Človeški konektom ali kakšne so zveze v naših možganih
Blaž Koritnik
Niko Lah
Torkove delavnice za osnovnošolce
Mateja Drolec Novak, Vid V. Vodušek
Da ne pozabim! Tehnike za pomladitev spomina
Klara Tostovršnik, Hana Hawlina
Površina socialne nevroznanosti
Manuel Kuran
Clarity - bistri možgani Karla Deisserotha
Gregor Belušič
Barbara Gnidovec Stražišar
Bojana Žvan
Nevroplastičnost po možganski kapi
Marjan Zaletel
Klinično psihološka obravnava pacientov po možganski kapi in podpora pri vračanju na delovno mesto
Barbara Starovasnik Žagavec
Možgani: organ, s katerim ljubimo
Andraž Matkovič
Marija Šoštarič Podlesnik
Gibalno-kognitivna vadba: praktična delavnica
Mitja Gerževič, Marina Dobnik
Anton Grad
Nevrologija, imunologija, psihiatrija …
Bojan Rojc
Andraž Stožer, Janez Bregant
Dominika Novak Pihler
Možganska kap – »kako ostati v omrežju?«
Nina Ozimic
Klara Tostovršnik
eSinapsa, 2014-8
Znotrajžilno zdravljenje možganskih anevrizem
Tamara Gorjanc, Dimitrij Lovrič
Obravnava hladnih možganskih anevrizem
Bojana Žvan, Janja Pretnar Oblak
Ali deklice z Rettovim sindromom govorijo z očmi?
Anka Slana, Urška Slana
Progresivna multifokalna encefalopatija
Urša Zabret, Katarina Šurlan Popovič
Ne ubijaj – poskusi na živalih
Martina Perše
Poizkusi na živalih - za in proti
Simon Horvat
eSinapsa, 2015-9
Kako deluje navigacijski sistem v naših možganih
Simon Brezovar
Vsakodnevno delo slepe osebe / s slepo osebo
Denis Kamnar
Uroš Marušič
Manca Tekavčič Pompe
Toni Pustovrh
Marko Hawlina
Od svetlobe do podobe ali kako vidijo svet naši možgani
Simon Brezovar
Janja Hrastovšek
Zala Kurinčič
Pogledi na mejno osebnostno motnjo
Jerica Radež, Peter Kapš
Uvid kot socialno psihološki fenomen
Vid Vodušek
Uvod v vidno-prostorske funkcije s praktičnimi primeri
Ana Bujišić, Sanja Roškar
eSinapsa, 2015-10
Difuzijsko magnetnoresonančno slikanje
Rok Berlot
Katja Pavšič
Radiološko izolirani sindrom - ali ga moramo poznati?
Matej Vouk, Katarina Šurlan Popovič
Kako izgledajo možgani, ki govorijo več jezikov?
Gašper Zupan
Nov pristop v rehabilitaciji - terapija s pomočjo psa
Mateja Drljepan
Pogled v maternico z magnetnoresonančno preiskavo
Taja Jordan, Tina Vipotnik Vesnaver
Saša Zorjan
Saša Zorjan
Nevroestetika: ko nevroznanost obišče galerijo
Anja Voljavec, Hana Hawlina, Nika Vrabič
Ali so psihogeni neepileptični napadi res psihogeni?
Saška Vipotnik, Gal Granda
Kako nam lahko glasna glasba »vzame« sluh in povzroči tinitus
Nejc Steiner, Saba Battelino
eSinapsa, 2016-11
Mara Bresjanac
Kako ultrazvok odpira pot v možgane
Kaja Kolmančič
Kako je epigenetika spremenila nevroznanost
Metka Ravnik Glavač
Ondinino prekletstvo ali sindrom prirojene centralne hipoventilacije
Katja Pavšič, Barbara Gnidovec Stražišar, Janja Pretnar Oblak, Fajko F. Bajrović
Zika virus in magnetnoresonančna diagnostika nepravilnosti osrednjega živčevja pri plodu
Rok Banko, Tina Vipotnik Vesnaver
Motnje ravnotežja otrok in odraslih
Nejc Steiner, Saba Battelino
eSinapsa, 2016-12
Vloga magnetnoresonančne spektroskopije pri obravnavi možganskih tumorjev
Gašper Zupan, Katarina Šurlan Popovič
Tiskanje tridimenzionalnih modelov v medicini
Andrej Vovk
Aleš Oblak
Kevin Klarič
Sinestezija: umetnica, ki ne želi odrasti
Tisa Frelih
Računska psihiatrija: od nevroznanosti do klinike
Nastja Tomat
Kognitivni nadzor: od vsakdanjega življenja do bolezni
Vida Ana Politakis
eSinapsa, 2017-13
Internet: nadgradnja ali nadomestek uma?
Matej Perovnik
Vloga črevesnega mikrobioma pri odzivu na stres
Vesna van Midden
Stres pušča posledice tako na človeškem kot živalskem organizmu
Jasmina Kerčmar
Prikaz normalne anatomije in bolezenskih stanj obraznega živca z magnetno resonanco
Rok Banko, Matej Vrabec
Psihedelična izkušnja in njen zdravilni potencial
Anja Cehnar, Jona Basle
Vpliv hiperglikemije na delovanje možganov
Jasna Šuput Omladič, Simona Klemenčič
Nevrofibromatoza: napredujoče obolenje centralnega in perifernega živčevja
Nejc Steiner, Saba Battelino
Fenomen žrtvenega jagnja v dobi interneta
Dolores Trol
Tesnoba staršev in strategije spoprijemanja, ko pri otroku na novo odkrijejo epilepsijo
Daša Kocjančič, Petra Lešnik Musek, Vesna Krkoč, David Gosar
eSinapsa, 2017-14
Zakaj ne zapeljem s ceste, ko kihnem?
Anka Slana Ozimič, Grega Repovš
Nobelova nagrada za odkritje molekularnih mehanizmov nadzora cirkadianih ritmov
Leja Dolenc Grošelj
Možgani pod stresom: od celic do duševnih motenj
Nastja Tomat
Na sledi prvi vzročni terapiji Huntingtonove bolezni
Danaja Metul
Razlike med spoloma pri Parkinsonovi bolezni
Kaja Kolmančič
eSinapsa, 2018-15
Susceptibilno poudarjeno magnetnoresonančno slikanje pri bolniku z ALS
Alja Vičič, Jernej Avsenik, Rok Berlot
Sara Fabjan
Reverzibilni cerebralni vazokonstrikcijski sindrom – pot do diagnoze
Maja Cimperšek, Katarina Šurlan Popovič
Liam Korošec Hudnik
Kognitivno funkcioniranje pri izgorelosti
Marina Horvat
eSinapsa, 2019-16
Maša Čater
Saša Koprivec
Infekcije osrednjega živčnega sistema s flavivirusi
Maja Potokar
Raziskava: Kako depresija vpliva na kognitivne sposobnosti?
Vida Ana Politakis
Razvoj depresije pri otrocih z vidika navezovalnega vedenja
Neža Grgurevič
Sonja Prpar Mihevc
Umetno inteligentna nevroznanost: srečanje nevronskih mrež in možganske fiziologije
Kristijan Armeni
Čebelji strup pri preventivi nevrodegenerativnih bolezni in priložnost za klinično prakso
Matjaž Deželak
eSinapsa, 2019-17
IgG4+ – skupni imenovalec diagnoz iz preteklosti
Cene Jerele, Katarina Šurlan Popovič
Nov molekulski mehanizem delovanja ketamina v astrocitih
Matjaž Stenovec
Praktični pristop k obravnavi utrujenosti in motenj spanja pri bolnikih z multiplo sklerozo
Nik Krajnc, Leja Dolenc Grošelj
Jure Pešak
eSinapsa, 2020-18
Bolezni spektra anti-MOG pri odraslih
Nik Krajnc
Samomor pod lupo nevroznanosti
Alina Holnthaner
eSinapsa, 2020-19
Ob mednarodnem dnevu znakovnih jezikov
Anka Slana Ozimič
Teorija obetov: kako sprejemamo tvegane odločitve
Nastja Tomat
Sara Fabjan
Matjaž Deželak
Nina Stanojević, Uroš Kovačič
Od človeških nevronov do možganskih organoidov – nova obzorja v nevroznanosti
Vesna M. van Midden
Splošna umetna inteligenca ali statistične jezikovne papige?
Kristijan Armeni
Zunajcelični vezikli kot prenašalci zdravilnih učinkovin preko krvno-možganske prepreke
Saša Koprivec
Matjaž Deželak
eSinapsa, 2021-20
Migrena: starodavna bolezen, sodobni pristopi k zdravljenju
Eva Koban, Lina Savšek
Zgodnji razvoj socialnega vedenja
Vesna Jug
Nastja Tomat
Mikrosplet: povezovanje preko mikrobioma
Tina Tinkara Peternelj
Stimulacija možganov kot način zdravljenja depresije
Saša Kocijančič Azzaoui
eSinapsa, 2021-21
eSinapsa, 2022-22
Sodobni vidiki motenj hranjenja
Karin Sernec
Ples in gibalni dialog z malčki
Neva Kralj
Atul Gawande
Jezikovna funkcija pri Alzheimerjevi bolezni
Gašper Tonin
Dostava terapevtikov preko krvno-možganske pregrade
Matjaž Deželak
eSinapsa, 2022-23
Akutni ishemični infarkt hrbtenjače pri zdravih otrocih – kaj lahko pove radiolog?
Katarina Šurlan Popovič, Barbara Šijaković
eSinapsa, 2023-24
Možganska omrežja pri nevrodegenerativnih boleznih
Tomaž Rus, Matej Perovnik
Morske živali kot navdih za nevroznanstvenike: morski konjiček, morski zajček in klobučnjak
Tina Bregant
Metoda Feldenkrais: gibanje in nevroplastičnost
Mateja Pate
Etično naravnana animalna nevroznanost
Maša Čater
Helena Motaln, Boris Rogelj
eSinapsa, 2023-25
Urban Košak, Damijan Knez, Anže Meden, Simon Žakelj, Jurij Trontelj, Jure Stojan, Maja Zakošek Pipan, Kinga Sałat idr.
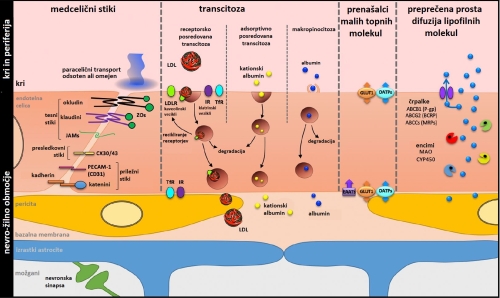
Prekrvavitev možganov in s tem izmenjava snovi med možgani in ostalimi tkivi ter organi je visoko nadzorovana in natančno uravnavana. Takšno zaščito možganom omogoča na poseben način organizirana stena kapilar iz endotelnih celic, pericitov in izrastkov astrocitov, debeline 10–50 μm, imenovana krvno-možganska pregrada (angl. Blood-Brain Barrier, BBB) 1 (Slika 1). Njena ocenjena površina, namenjena izmenjavi snovi med krvjo in možgani, je 12–18 m2 2, na skupni dolžini približno 650 km 3, kar praktično predstavlja celoten stik med možgani in krvožiljem.
Vendar obstajajo nekatere izjeme. Na nekaterih predelih obventrikularnih organov (angl. Circumvetricular Organs) in koroidnega pleksusa je BBB neizrazita ali celo odsotna in ti predeli omogočajo prosto difuzijo snovi med krvjo in možgani 1. Teoretično se možnost dostave zdravil preko teh področij zdi enostavna, vendar zaradi različnih razlogov praktičnih uspehov še ni bilo. Nasprotno je v področjih BBB transcitozni prenos snovi omejen z visoko selektivnimi encimi, receptorji, transmembranskimi prenašalci in raznimi črpalkami 1, medcelični prost pretok snovi pa preprečen s tesnimi stiki v povezavi s priležnimi in presledkovnimi stiki 4. Seveda pa se tudi BBB po strukturi in lastnostih razlikuje vzdolž žilja 5, največje razlike so med BBB v arteriolah, venulah in kapilarah 3.
Pri obravnavi lastnosti BBB se je potrebno zavedati, da izmenjava snovi preko nje ne poteka na nek avtomatiziran oziroma vnaprej določen in nespremenljiv način, ampak je odvisna od aktivnosti in potreb nevronov in ostalih možganskih celic. Možganski periciti namreč segajo vse do bazalne lamine BBB (Slika 1) in aktivno komunicirajo z njenimi endotelnimi celicami; skupno predstavljajo kar slabo tretjino nelumenske strani BBB 6. Podobno komunikacijsko vlogo imajo tudi izrastki astrocitov 7, mikroglije in oligodendrocitov 8.
Biološki namen BBB je uravnavanje metabolne homeostaze ter zaščita pred patogeni in škodljivimi ksenobiotiki. Ravno ta njena visoka selektivnost pa farmaciji in medicini predstavlja poseben izziv pri načrtovanju zdravil in postopkov zdravljenja bolezni možganov. Skladno s tem se zadnja desetletja raziskave usmerjajo v iskanje načinov kako »pretentati« BBB, da bo dopuščala vstop izbranim molekulam.
Dejavniki, ki vplivajo na prenos zdravil preko krvno-možganske pregrade
Starost je pri vsakem zdravljenju in medicinskem posegu dejavnik, ki ga je najprej potrebno upoštevati, saj se celice in tkiva skozi življenje spreminjajo kot posledica oksidativnega stresa, epigenetskih sprememb, genomske nestabilnosti, krajšanja telomer, motenj celične signalizacije, spremenjenega vnetnega odziva in izgube sposobnosti celične delitve 9. Tudi struktura in funkcija BBB s starostjo slabita, kar je v pretežni meri posledica manjše ekspresije jedrnega proteina Sirtuin-1 10. Študije na živalskih modelih kažejo tudi od starosti odvisno spremenjeno izražanje nekaterih genov v astrocitih 11 in pericitih 12, kar ima za posledico zmanjšano permeabilnost BBB.
Biološki spol vpliva na lastnosti BBB preko različne ekspresije membranskega P-glikoproteina 1, katerega naloga je, da iz celice črpa tuje snovi. Njegova aktivnost je nižja pri ženskah v primerjavi z moškimi primerljive starosti 13, odvisna pa je tudi od starosti, saj se pri ženskah s starostjo ne zmanjšuje bistveno, pri moških pa se 14. Spol vpliva tudi na farmakokinetiko, predvsem na eliminacijo zdravila iz možganov, kar je bilo pokazano s približno 4-krat daljšim razpolovnim časom letrozola pri ženskah kot pri moških 15.
Način vnosa zdravila je ključen dejavnik biološke dostopnosti zdravila v možganih. Najmanj ugodna je oralna aplikacija, saj z njo zdravilo preide v sistemski krvni obtok posredno preko jeter, kjer se zgodi prva stopnja metabolizma, t. i. »učinek prvega prehoda« (angl. First Pass Effect). Prednost rektalne, intravenske, intramuskularne, pulmonalne, bukalne in sublingualne poti je, da preko njih zdravilo vstopi neposredno v sistemski krvni obtok, vendar mora učinkovina še vedno prečkati BBB. Z vidika dostave zdravil v možgane imata veliko prednost intranazalna in intratekalna aplikacija, saj z njima zdravilo zaobide BBB in pride neposredno v možgane 16. V primerjavi z intratekalno aplikacijo, pri kateri zdravilo vbrizgamo v subarahnoidni prostor ali neposredno v hrbtenjačni kanal, je intranazalna aplikacija precej bolj enostavna in sprejemljiva za bolnika.
Sodobni načini prenosa zdravil preko krvno-možganske pregrade
Farmacevtski razvoj varnih in učinkovitih zdravil nima nobenega smisla, če zdravila ne zmoremo vnesti na mesto delovanja. Lahko najdemo idealno zdravilo, visoko učinkovito in brez neželenih učinkov, a je popolnoma neuporabno, če ne najdemo tudi varnega načina za njegovo učinkovito dostavo na mesto, kjer naj se terapevtski učinek zgodi. Dostava zdravil temelji na njihovi farmakokinetiki in farmakodinamiki in je eno izmed hitreje spreminjajočih se področij. V nadaljevanju bomo predstavili trenutno aktualne načine tarčne dostave zdravil preko BBB, z izjemo zunajceličnih veziklov, o katerih smo v eSiNAPSI že pisali (povezava do članka).
Prilagajanje fizikalno-kemijskih lastnosti učinkovin je najbolj elegantna rešitev pri načrtovanju zdravil, namenjenih prehodu BBB. Ker njena struktura zaradi tesnih stikov med soležnimi endotelnimi celicami sama po sebi ne dopušča prehajanja molekul, je transcelični prenos s pasivno difuzijo prva izbira. Pogojuje jo pet fizikalno-kemijskih parametrov: molska masa, lipofilnost, polarna površinska razporeditev, možnost tvorbe vodikovih vezi in površinski naboj 17. Splošno sprejeto je, da je velika verjetnost za prehod BBB pri učinkovinah, ki imajo molsko maso največ 500 Da, največ 5 donorjev in 10 akceptorjev vodikovih vezi in log P koeficient razporeditve oktanol-voda največ 5 17. Praktične izkušnje kažejo, da je transcelično difuzijo le redko mogoče doseči brez negativnega vpliva na ostale farmakološke lastnosti. Tipski primer je terciarna-butil ester oblika klorambucila (CAS: 305-03-3), ki sicer prehaja v možgane v 7-krat večji koncentraciji, vendar ta kemijska modifikacija bistveno vpliva tudi na njegovo razporeditev v druge organe in na jakost vezave na plazemske proteine 18. Fizikalno-kemijske lastnosti učinkovin so preveč pomembne za njihovo delovanje, zato se običajno poslužujemo ostalih načinov za prenos preko BBB.
Nanodelci so trdni koloidni delci velikosti 1 – 100 nm, raznolike kemijske sestave in oblik. Začetki njihove uporabe kot prenašalce preko BBB segajo v 90. leta prejšnjega stoletja. Najpogosteje uporabljeni nanodelci so 19:
- Poli(butilcianoakrilat) (PBCA),
- ciklodekstrini (CDX),
- poli(ε-kaprolakton) (PCL),
- poli(lakto-ko-glikolna kislina) (PLGA),
- poli(mlečna kislina) PLA,
- hitozan-lecitin,
- zlato in
- silicij.
Zdravilno učinkovino v/na nanodelec raztopimo, dispergiramo, enkapsuliramo, ujamemo ali vežemo. Nanodelci ugodno vplivajo na usodo zdravila na poti v možgane, s tem da podaljšajo njegovo življenjsko dobo v telesu in neposredno olajšajo prehod preko BBB; vse to v odvisnosti od njihove velikosti, oblike in površinskega naboja 20.
Prvi uspešen primer uporabe nanodelcev za prenos zdravila v možgane je bil 700 Da velik heksapeptidni analgetik dalargin, adsorbiran na površino PBCA, prekrit s polisorbatom PS80 21. Kasneje so na podoben način dostavili še loperamid, doksorubicin in tubokurarin. Mehanizem prehoda BBB sprva ni bil poznan, kasnejše raziskave pa so pokazale, da ne gre za specifičen mehanizem prehoda, niti ne za kakšno pospešeno nespecifično prehajanje BBB, ampak je vezava dalargina na nanodelce zmanjšala njegovo jetrno presnovo 22. S tem je razpolovni čas zdravila v krvi daljši in je posledično dlje časa v stiku z BBB, to pa posredno poveča njegovo možgansko razporeditev, ne da bi dejansko prišlo do izboljšanega prehajanja endotela BBB 23. Kasneje so tako formulirane učinkovine našli praktično v vseh organih, saj takšen prehod velja za vsa endotelna tkiva; s PS80 prekriti PBCA-nanodelci namreč nase vežejo apolipoproteine, te pa endotelne celice privzamejo preko LDL-receptorske endocitoze 24.
Ciklodekstrini so druga zanimiva skupina nanodelcev, saj so s strani glavnih regulatornih institucij (PMDA, FDA, EMA, EFSA) večinoma sprejeti kot varne naravne snovi, dovoljene v živilski in farmacevtski industriji. Ciklodekstrini so krožni oligosaharidi iz 6 (α-), 7 (β-) ali 8 (γ-ciklodekstrini) molekul β-D-glukopiranoze, vezanih z α(1->4) vezmi (Slika 2), zaradi česar zavzamejo obliko votlega prisekanega stožca s polarno zunanjostjo in nepolarno notranjostjo 25. Mehanizmi prehoda ciklodekstrinov še niso povsem pojasnjeni, najverjetneje pa je ključna njihova sposobnost vezave holesterola, kar povzroči t. i. fuzogenično obliko endocitoze in s tem obhod mimo iztočnih črpalk P-gp in BCRP 26 27. Previdnost je potrebna le pri visokih odmerkih v kombinaciji z intravensko aplikacijo zaradi citotoksičnosti kot posledica privzema holesterola iz celičnih membran 27.
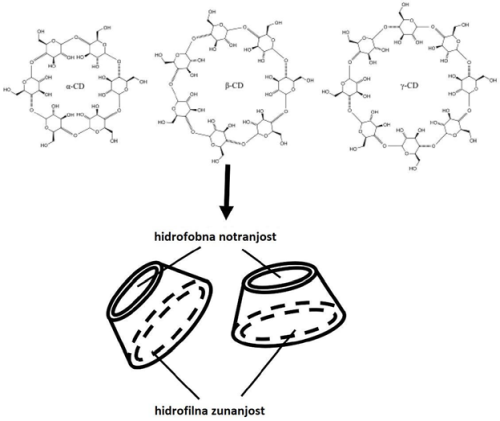
Slika 2: Strukturna formula nanodelcev ciklodekstrinov s ponazoritvijo 3D oblike votlega prisekanega stožca s polarno zunanjostjo in nepolarno notranjostjo (povzeto po 5).
Biološko razgradljivi nanodelci PLGA so prav tako obetajoči za prenos različnih molekul preko BBB, tudi proteinov in nukleinskih kislin (Slika 3). Nadzora njihove velikosti 100–350 nm in površinskega naboja sta enostavna, omogočajo različne kovalentne modifikacije (npr. fluorofori, supermagnetni železov oksid), res pa je, da lahko vežejo relativno malo tovora 28. Uporaba različnih fluoroforov v kombinaciji s fluorescenčnim, MRI- in PET-slikanjem je pokazalo zelo nizko prehajanje intaktnih nanodelcev PLGA preko BBB, zato je njihova modifikacija praktično neizogibna 29. Prvi uspešen primer je preplastitev nanodelcev PLGA s poloksamerom 188 in uspešna dostava BDNF v mišje možgane 30, drugi pa vezava glikoziliranega peptida g7 (analog enkefalina) in dostava loperamida preko BBB v miših 31.
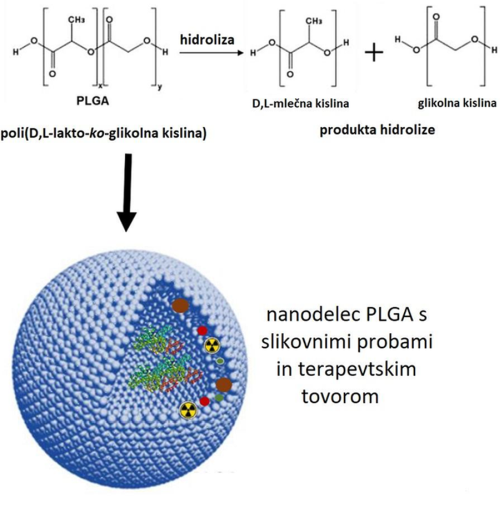
Slika 3: Strukturna formula in 3D prikaz nanodelca PLGA (povzeto po 5) x, y – poljubno število monomerov.
Liposomi in miceli so dvoslojni in enoslojni sferični vezikli širokega razpona velikosti (250 nm–2,5 μm) iz fosfolipidov in holesterola, pri čemer je notranjost liposomov hidrofilna, notranjost micelov pa hidrofobna 32. Njihova zgradba še zdaleč ni omejena na fosfolipide in holesterol, v poštev pride ogromno drugih dolgoverižnih amfipatičnih molekul, mogoče so tudi njihove kombinacije, zaradi česar lahko ustvarimo liposome in micele mnogoterih pestrosti. Kot uporabni so se izkazali pri dostavi zdravil preko BBB pri modelu ishemične kapi, kjer so opazili transceličen in/ali paraceličen prehod BBB, odvisno od časa aplikacije po ishemični kapi 33. Drugi primer dobre prakse je uporaba PEG-iliranih in s peptidom HAIYPRH (T7) konjugiranih liposomov za prenos ZL006 preko BBB 34. Razporeditev ZL006 v možganih je bila res signifikantna, kot se je izkazalo ravno zaradi (T7) peptida HAIYPRH, ki je ligand transferinskih receptorjev.
Usmerjen ultrazvok v kombinaciji z mikromehurčki je primer fizikalnega pristopa za začasno spremembo zgradbe in integritete BBB. Princip deluje na predhodni intravenski aplikaciji mikromehurčkov, nato pa z usmerjenim ultrazvokom nizke jakosti (okoli 200 kHz) povzročimo njihovo oscilacijo v področju BBB in s t. i. akustično kavitacijo začasno razprtje tesnih stikov endotelnih celic kapilar 35. Sestava in lastnosti tako zrahljane BBB se načeloma povrnejo v 20–30 ur, brez opaznih fizioloških in nevroloških posebnosti. Tehnika kot taka je precej nova, so pa že bile pokazane uspešne uporabe: v primeru Alzheimerjeve bolezni 15–70% večja prepustnost BBB 35, v primeru možganskega glioma 15–50% večji prehod sistemskega kemoterapevtika v možgane 36 in v primeru intranazalnega vnosa dekstrana 8-krat večji prehod preko BBB 37.
Do z receptorji posredovane transcitoze pride, ko neka učinkovina aktivira endocitozne receptorje luminalnih endotelnih celic. Učinkovina ostane vezana na receptor, takšen konjugat pa se z endocitoznim veziklom intakten prenese preko celice in se s fuzijo plazmaleme izloči, s čimer zaobide celoten molekularni ustroj celice 38. Velika prednost tega pristopa je, da za prehod BBB uporabimo celicam lastne mehanizme in da se prenesene molekule pri prenosu fizikalno-kemijsko ne spremenijo. Izziv pa ostaja priprava takega tovora, da ga bodo endocitozni receptorji prepoznali. Raziskave na tem področju so že uspešno prešle in vitro in in vivo študije na živalskih modelih, trenutno potekata dve klinični študiji za prenos pabinafusp-α preko transferinskega receptorja 39 in valanafusp-α preko inzulinskega receptorja 40.
Modulacija encimov z agonisti/antagonisti jedrnih receptorjev je podobno kot receptorska transcitoza zanimiva, saj malo ali nič ne prizadene normalno delovanje celic. Endotelne celice BBB na površini izražajo različne jedrne receptorje, ki vplivajo na ekspresijo encimov za metabolizem ksenobiotikov (npr. encimi skupine CYP) 41. Dobro poznana je vezava receptorjev za androstan in pregnan X na promotor gena CYP2C v človeški BBB 42. Podobno je utišanje glukokortikoidnega receptorja zmanjšalo CYP3A4 na proteinskem nivoju in posledično je več antiepileptičnega zdravila fentoin prišlo v možgane 41. Podobnih uspešnih raziskav je sicer kar nekaj 43 44 45, vendar ne smemo spregledati, da so podobni (če ne celo isti) receptorji po vsej verjetnosti izraženi tudi v celicah drugih tkiv in organov, kar pa vsekakor ni zaželeno.
Zaključek
Uvod zaključka naj bo realistično pesimističen: zaenkrat še nismo našli terapevtskega načina za zdravljenje nevrodegenerativnih bolezni s sprejemljivimi neželenimi učinki za kateregakoli bolnika. V tem prispevku smo opisali tako vpliv izhodiščnih dejavnikov, ki vplivajo na uspešnost zdravljenja bolezni možganov, kot tudi vpliv načinov vnosa terapevtikov v možgane bolnikov. Univerzalnega biokemijsko-fiziološkega pristopa ni, zato je v praksi ključno klinično usmerjanje zdravljenja vsakega posameznika s strani usposobljenega zdravnika na osnovi njegove sprotne diagnoze.
Z vidika prehoda zdravil preko BBB si vsekakor želimo več kakovostnih študij ter spoznanj o tem, kako konkretni terapevtiki prehajajo BBB in kako bi to prehajanje lahko izboljšali. In to na način, da ostala tkiva in organi ne bi bili prizadeti, želeno zdravilo pa bi v možganih opravilo svojo terapevtsko vlogo.
-
___
-
Abbott N. J., Patabendige A. A., Dolman D. E., Yusof S. R., Begley D. J. Structure and function of the blood-brain barrier. Neurobiology of Disease, 2010;37:13-25. ↩
-
Cecchelli R., Berezowski V., Lundquist S., Culot M., Renftel M., Dehouck M.P., Fenart L. Modelling of the blood-brain barrier in drug discovery and development. Nature Reviews Drug Discovery, 2007;6:650-661. ↩
-
Ge S., Song L., Pachter J. S. Where is the blood-brain barrier really? Journal of Neuroscience Research, 2005;79:421-427. ↩
-
Saint-Pol J., Gosselet F., Duban-Deweer S., Pottiez G., Karamanos Y. Targeting and crossing the blood-brain barrier with extracellular vesicles. Cells, 2020;9:851-863. ↩
-
Gosselet F., Loiola R., Roig A., Rosell A., Culot M. Central nervous system delivery of molecules across the blood-brain barrier. Neurochemistry International, 2021;144:104952. ↩
-
Daneman R., Zhou L., Kebede A. A., Barres B. A. Pericytes are required for blood-brain barrier integrity during embryogenesis. Nature, 2010;468:562-566. ↩
-
Berezowski V., Landry C., Dehouck M. P., Cecchelli R., Fenart L. Contribution of glial cells and pericytes to the mRNA profiles of P-glycoprotein and multidrug resistance-associated proteins in an in vitro model of the blood-brain barrier. Brain Res.earch, 2004;1018:1-9. ↩
-
Neuwelt E. A. Mechanisms of disease: the blood-brain barrier. Neurosurgery, 2004;54:131-140. ↩
-
Mattson M. P., Arumugam T. Hallmarks of brain aging: adaptive and pathological modification by metabolic states. Cell Metabolism, 2018;27:1176-1199. ↩
-
Stamatovic S. M., Martinez-Revollar G., Hu A., Choi J., Keep R. F., Andjelkovic A. V. Decline in Sirtuin-1 expression and activity plays a critical role in blood-brain barrier permeability in aging. Neurobiology of Disease, 2018;126:105-116. ↩
-
Souza D. G., Bellaver B., Raupp G. S., Souza D. O., Quincozes-Santos, A. Astrocytes from adult Wistar rats aged in vitro show changes in glial functions. Neurochemistry International, 2015;90:93-97. ↩
-
Bell R. D., Winkler E. A., Sagare A. P., Singh I., La Rue B., Deane R., Zlokovic B. V. Pericytes control key neurovascular functions and neuronal phenotype in the adult brain and during brain aging. Neuron, 2010;68:409-427. ↩
-
Bebawy M., Chetty M. Gender differences in p-glycoprotein expression and function: Effects on drug disposition and outcome. Current Drug Metabolism, 2009;10:322-328. ↩
-
Van Assema D. M., Lubberink M., Boellaard R., Schuit R. C., Windhorst, A. D., Scheltens P., Lammertsma A. A., van Berckel B. N. P-glycoprotein function at the blood-brain barrier: Effects of age and gender. Molecular Imaging and Biology, 2012;14:771-776. ↩
-
Arora P., Gudelsky G., Desai P. B. Gender-based differences in brain and plasma pharmacokinetics of letrozole in sprague-dawley rats: Application of physiologically-based pharmacokinetic modeling to gain quantitative insights. PLoS ONE, 2021;16:e0248579. ↩
-
Liu X. Clinical trials of intranasal delivery for treating neurological disorders – A critical review. Expert Opinion on Drug Delivery, 2011;8:1681-1690. ↩
-
Lipinski C. A., Lombardo F., Dominy B. W., Feeney P. J. Experimental and computational approaches to estimate solubility and permeability in drug discovery and development settings. Advanced Drug Delivery Reviews, 2001;46:3-26. ↩
-
Greig N. H., Daly E. M., Sweeney D. J., Rapoport S. I. Pharmacokinetics of chlorambucil-tertiary butyl ester, a lipophilic chlorambucil derivative that achieves and maintains high concentrations in brain. Cancer Chemotherapy and Pharmacology, 1990;25:320-325. ↩
-
Fisher D. G., Price R. J. Recent advances in the use of focused ultrasound for magnetic resonance image-guided therapeutic nanoparticle delivery to the central nervous system. Frontiers in Pharmacology, 2019;10:1348. ↩
-
Zhang Y., Liu A. T., Cornejo Y. R., Van Haute D., Berlin J. M. Systematic comparison of in vitro cell uptake and in vivo biodistribution for three classes of gold nanoparticles with saturated PEG coatings. PloS One 2020;15:e0234916. ↩
-
Kreuter J., Alyautdin R. N., Kharkevich D. A., Ivanov A. A. Passage of peptides through the blood-brain barrier with colloidal polymer particles (nanoparticles). Brain Research, 1995;674:171-174. ↩
-
Schroeder U., Schroeder H., Sabel B. A. Body distribution of 3H-labelled dalargin bound to poly(butyl cyanoacrylate) nanoparticles after i.v. injections to mice. Life Sciences, 2000;66:495-502. ↩
-
Ramge P., Unger R. E., Oltrogge J. B., Zenker D., Begley D., Kreuter J., Von Briesen H. Polysorbate-80 coating enhances uptake of polybutylcyanoacrylate (PBCA)-nanoparticles by human and bovine primary brain capillary endothelial cells. European Journal of Neuroscience, 2000;12:1931-1940. ↩
-
Kreuter J., Shamenkov D., Petrov V., Ramge P., Cychutek K., Koch-Brandt C., Alyautdin R. Apolipoprotein-mediated transport of nanoparticle-bound drugs across the blood-brain barrier. Journal of Drug Targeting, 2002;10:317-325. ↩
-
Coisne C., Tilloy S., Monflier E., Wils D., Fenart L., Gosselet F. Cyclodextrins as emerging therapeutic tools in the treatment of cholesterol-associated vascular and neurodegenerative diseases. Molecules, 2016;21:1748. ↩
-
Tilloy S., Monnaert V., Fenart L., Bricout H., Cecchelli R., Monflier E. Methylated beta-cyclodextrin as P-gp modulators for deliverance of doxorubicin across an in vitro model of blood-brain barrier. Bioorganic & Medicinal Chemistry Letters, 2006;16:2154-2157. ↩
-
Coisne C., Hallier-Vanuxeem D., Boucau M. C., Hachani J., Tilloy S., Bricout H., Monflier E., Wils D., Serpelloni M., Parissaux X., Fenart L., Gosselet F. β-cyclodextrins decrease cholesterol release and ABC-associated transporter expression in smooth muscle cells and aortic endothelial cells. Frontiers in Physiology, 2016;7:185. ↩
-
Park K., Skidmore S., Hadar J., Garner J., Park H., Otte A., Soh B. K., Yoon G., Yu D., Yun Y., Lee B. K., Jiang X., Wang Ynjectable, long-acting PLGA formulations: analyzing PLGA and understanding microparticle formation. Journal of Controlled Release, 2019;304:125-134. ↩
-
Zhang Y., Garcia-Gabilondo M., Grayston A., Feiner I. V. J., Anton-Sales I., Loiola R. A., Llop J., Ramos-Cabrer P., Barba I., Garcia-Dorado D., Gosselet F., Rosell A., Roig A. PLGA protein nanocarriers with tailor-made fluorescence/MRI/PET imaging modalities. Nanoscale, 2020;12:4988-5002. ↩
-
Khalin I., Alyautdin R., Wong T. W., Gnanou J., Kocherga G., Kreuter J. Brain-derived neurotrophic factor delivered to the brain using poly (lactide-co-glycolide) nanoparticles improves neurological and cognitive outcome in mice with traumatic brain injury. Drug Delivery, 2016;23:3520-3528. ↩
-
Vilella A., Belletti D., Sauer A. K., Hagmeyer S., Sarowar T., Masoni M., Stasiak N., Mulvihill J. J. E., Ruozi B., Forni F., Vandelli M. A., Tosi G., Zoli M., Grabrucker A. M. Reduced plaque size and inflammation in the APP23 mouse model for Alzheimer’s disease after chronic application of polymeric nanoparticles for CNS targeted zinc delivery. Journal of Trace Elements in Medicine and Biology, 2018;49:210-221. ↩
-
Akbarzadeh A., Rezaei-Sadabady R., Davaran S., Joo S. W., Zarghami N., Hanifehpour Y., Samiei M., Kouhi M., Nejati-Koshki K. Liposome: Classification, preparation, and applications. Nanoscale Research Letters, 2013;8:102. ↩
-
Al-Ahmady Z. S., Jasim D., Ahmad S. S., Wong R., Haley M., Coutts G., Schiessl I., Allan S. M., Kostarelos K. Selective liposomal transport through blood brain barrier disruption in ischemic stroke reveals two distinct therapeutic opportunities. ACS Nano, 2019;13:12470-12486. ↩
-
Wang Z., Zhao Y., Jiang Y., Lv W., Wu L., Wang B., Lv L., Xu Q., Xin H. Enhanced anti-ischemic stroke of ZL006 by T7-conjugated PEGylated liposomes drug delivery system. Scientific Reports, 2015;5:12651. ↩
-
Rezai A. R., Ranjan M., D’Haese P.-F., Haut M. W., Carpenter J., Najib U., Mehta R. I., Chazen J. L., Zibly Z., Yates J. R., et al. Noninvasive hippocampal blood-brain barrier opening in Alzheimer’s disease with focused ultrasound. Proceedings of the National Academy of Sciences, 2020;117:9180-9182. ↩
-
Mainprize T., Lipsman N., Huang Y., Meng Y., Bethune A., Ironside S., Heyn C., Alkins R., Trudeau M., Sahgal A., et al. Blood-brain barrier opening in primary brain tumors with non-invasive MR-guided focused ultrasound: A clinical safety and feasibility study. Scientific Reports, 2019;9:321. ↩
-
Chen H., Chen C. C., Acosta C., Wu S. Y., Sun T., Konofagou E. E. A new brain drug delivery strategy: Focused ultrasound-enhanced intranasal drug delivery. PLoS ONE, 2014;9:e108880. ↩
-
Tashima, T. Smart strategies for therapeutic agent delivery into brain across the blood–brain barrier using receptor-mediated transcytosis. Chemical and Pharmaceutical Bulletin; 2020;68:316-325. ↩
-
Okuyama T., Eto Y., Sakai N., Nakamura K., Yamamoto T., Yamaoka M., Ikeda T., So S., Tanizawa K., Sonoda H., et al. A phase 2/3 trial of pabinafusp alfa, IDS fused with anti-human transferrin receptor antibody, targeting neurodegeneration in MPS-II. Molecular Therapy, 2021;29:671-679. ↩
-
Giugliani R., Giugliani L., Poswar F. D. O., Donis K. C., Corte A. D., Schmidt M., Boado R. J., Nestrasil I., Nguyen C., Chen S., et al. Neurocognitive and somatic stabilization in pediatric patients with severe Mucopolysaccharidosis Type I after 52 weeks of intravenous brain-penetrating insulin receptor antibody-iduronidase fusion protein (valanafusp alpha): An open label phase 1-2 trial. Orphanet Journal Rare Diseases, 2018;13:110. ↩
-
Ghosh C., Hossain M., Mishra S., Khan S., Gonzalez-Martinez J., Marchi N., Janigro D., Bingaman W., Najm I. Modulation of glucocorticoid receptor in human epileptic endothelial cells impacts drug biotransformation in an in vitro blood-brain barrier model. Epilepsia, 2018;59:2049-2060. ↩
-
Ferguson S. S., Chen Y., LeCluyse E. L., Negishi M., Goldstein J. A. Human CYP2C8 Is transcriptionally regulated by the nuclear receptors constitutive androstane receptor, pregnane X receptor, glucocorticoid receptor, and hepatic nuclear factor 4α. Molecular Pharmacology, 2005;68:747-757. ↩
-
Canet G., Chevallier N., Zussy C., Desrumaux C., Givalois L. Central role of glucocorticoid receptors in Alzheimer’s disease and depression. Frontiers in Neuroscience, 2018;12:739. ↩
-
Loose D. S., Stover E. P., Feldman D. Ketoconazole binds to glucocorticoid receptors and exhibits glucocorticoid antagonist activity in cultured cells. The Journal of Clinical Investigation, 1983;72:404-408. ↩
-
Baglietto-Vargas D., Medeiros R., Martinez-Coria H., LaFerla F. M., Green K. N. Mifepristone alters amyloid precursor protein processing to preclude amyloid beta and also reduces tau pathology. Biological Psychiatry, 2013;74:357-366. ↩
DDr. Matjaž Deželak, univ. dipl. biol.
SiNAPSA, slovensko društvo za nevroznanost
Sprejeto: 2.9.2022
Objavljeno: 20.9.2022